Quanti di noi non hanno mai assaggiato una tavoletta di cioccolata, un ovetto, una pralina o una tazza fumante di cioccolata calda? Dopo quel morso o quel sorso, quasi sempre arriva una sensazione di benessere, un piccolo conforto che sembra andare oltre il semplice gusto. Non è un’illusione: dietro c’è la chimica.
Un po’ di storia
La storia del cioccolato affonda le sue radici ben prima dell’arrivo in Europa. Le prime tracce di utilizzo del cacao risalgono a più di tremila anni fa e sono legate alle civiltà dell’America centrale, a partire dagli Olmechi, che probabilmente furono i primi a coltivare e trasformare i semi di cacao. I Maya lo considerarono un dono divino: lo impiegavano nelle cerimonie religiose, lo offrivano agli dei e lo seppellivano persino nelle tombe come viatico per l’aldilà. Per loro, come più tardi per gli Aztechi, il cacao era anche moneta sonante: i semi servivano a pagare tributi e scambi, trasformando il frutto in una ricchezza tangibile oltre che simbolica. Ma il cioccolato di allora non aveva nulla a che vedere con la tavoletta dolce e cremosa che conosciamo: si trattava di una bevanda amara, densa, speziata con peperoncino o vaniglia, chiamata “xocolatl”, riservata a nobili e guerrieri e consumata come tonico energizzante e rituale.
Fu soltanto dopo la scoperta delle Americhe che il cacao attraversò l’Atlantico. Cristoforo Colombo ne raccolse alcuni semi, ma fu Hernán Cortés a comprenderne il valore osservandone l’uso tra gli Aztechi e a introdurlo in Spagna. Qui la bevanda subì la prima trasformazione decisiva: al posto del peperoncino, i cuochi di corte iniziarono ad aggiungere zucchero, cannella e vaniglia, rendendola più gradevole al palato europeo. Il cacao divenne così una moda raffinata, diffondendosi nelle corti e nelle case aristocratiche di tutta Europa.
La svolta arrivò nel XIX secolo, quando l’ingegno tecnico permise di trasformare la bevanda in un alimento solido. Nel 1828 l’olandese Coenraad Van Houten inventò una pressa capace di separare il burro di cacao dalla polvere, ottenendo un prodotto più fine e versatile. Qualche decennio più tardi, in Inghilterra, la ditta Fry & Sons creò la prima tavoletta di cioccolato, seguita a ruota dagli svizzeri che introdussero l’aggiunta del latte in polvere e, con Rodolphe Lindt, perfezionarono il processo di conching[1] che regalò al cioccolato la sua inconfondibile cremosità. In pochi decenni il cioccolato smise di essere un lusso per pochi, legato alle “chocolate houses” frequentate da aristocratici e mercanti, per diventare un piacere diffuso e accessibile, destinato a conquistare il mondo.
Un po’ di chimica del cioccolato
Il cioccolato non nasce dolce e vellutato: per arrivare alla tavoletta che conosciamo occorre un percorso fatto di trasformazioni chimiche complesse. Tutto comincia nelle piantagioni, dove le fave di cacao vengono fermentate dentro mucillagini ricche di zuccheri. Qui lieviti e batteri innescano una catena di reazioni che porta alla formazione dei precursori degli aromi: si liberano amminoacidi e peptidi, si producono acidi organici, e perfino piccole quantità di ammine biogene che contribuiranno al profilo sensoriale finale.
Dopo la fermentazione, le fave vengono essiccate al sole. Questo passaggio riduce l’umidità, stabilizza i chicchi e permette che le reazioni ossidative continuino a sviluppare colore e gusto, attenuando l’astringenza tipica del cacao fresco.
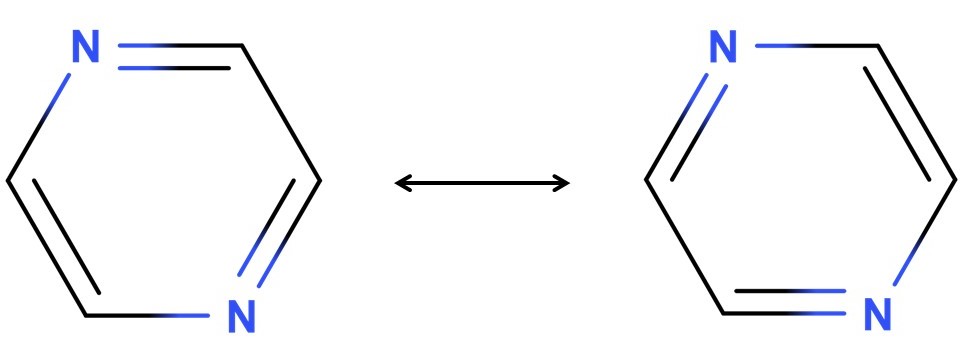
Il momento cruciale arriva con la tostatura, in fabbrica: a temperature tra 120 e 140 °C avvengono le celebri reazioni di Maillard, quelle stesse che danno la crosta dorata al pane e l’aroma alla carne arrostita. In questo caso, gli zuccheri reagiscono con gli amminoacidi liberati in fermentazione, generando un caleidoscopio di nuove molecole aromatiche: aldeidi, chetoni, acidi, ma soprattutto pirazine (Figura 1), responsabili del tipico profumo tostato e leggermente nocciolato del cioccolato. Anche la caramellizzazione degli zuccheri e l’ossidazione dei grassi contribuiscono a creare complessità.
Il burro di cacao, che rappresenta circa metà del peso della fava, è un capitolo a parte. La sua particolarità è la capacità di cristallizzare in diverse forme, o polimorfi, con punti di fusione diversi. Solo una di queste forme, detta β(V), conferisce al cioccolato la giusta consistenza: solido a temperatura ambiente, ma capace di sciogliersi in bocca a circa 30–32 °C. Per ottenere questo equilibrio serve un trattamento preciso chiamato temperaggio, che allinea i cristalli di burro di cacao nella struttura più stabile.
Infine, durante la fase di conching, la massa di cacao viene mescolata e riscaldata a lungo. In questo modo si eliminano acidi volatili indesiderati, si riduce l’astringenza dei polifenoli e si affinano le particelle solide, donando al cioccolato la sua texture setosa e il tipico effetto “melt-in-the-mouth”.
Il risultato di questa catena di trasformazioni è un alimento che non solo stimola i sensi con centinaia di molecole aromatiche, ma conserva anche composti bioattivi originari del cacao, come i flavonoidi (antiossidanti naturali), la teobromina e la caffeina, responsabili degli effetti stimolanti e di quel sottile senso di benessere che accompagna ogni morso.
La chimica del piacere
Come introdotto alla fine del paragrafo precedente, il cioccolato ci fa stare bene grazie a molecole quali:
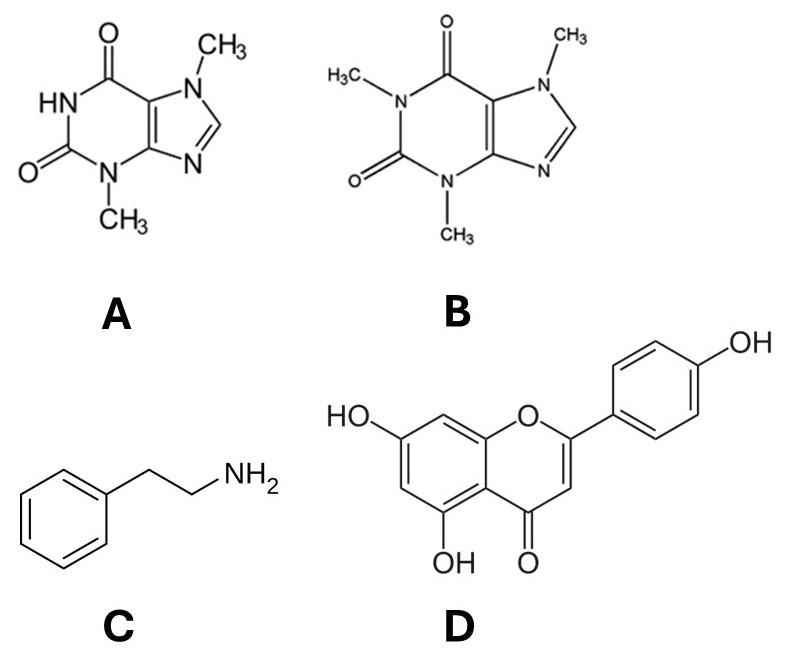
- Teobromina e caffeina (Figura 2A e 2B). Entrambi sono metilxantine, alcaloidi strutturalmente simili, che agiscono come antagonisti competitivi dei recettori dell’adenosina. Normalmente, l’adenosina riduce l’attività neuronale e favorisce sonnolenza e rilassamento; bloccarne i recettori ha quindi l’effetto opposto: maggiore vigilanza, riduzione della percezione della fatica, incremento della contrattilità muscolare e della frequenza cardiaca. La caffeina ha un’azione più potente e rapida, mentre la teobromina, presente in concentrazione più elevata nel cacao, ha effetti più blandi ma di lunga durata, con una marcata azione vasodilatatrice e diuretica.
- Feniletilammina (Figura 2C). È una ammina biogena derivata dalla decarbossilazione della fenilalanina. Ha una struttura simile alle amfetamine e agisce come modulatore neuromediatore: stimola il rilascio di dopamina e noradrenalina e inibisce la loro ricaptazione. Questo si traduce in un senso di euforia e piacere. Tuttavia, la sua emivita nell’organismo è brevissima (rapidamente degradata dalla monoaminoossidasi-B, MAO-B), per cui il suo contributo diretto è probabilmente modesto. Alcuni studi suggeriscono che gli effetti percepiti siano potenziati dalla contemporanea presenza di altre molecole del cacao, che ne modulano il metabolismo.
- Flavonoidi (Figura 2D). Sono polifenoli, in particolare flavanoli come epicatechina e catechina, abbondanti nel cacao. Il loro effetto principale riguarda l’endotelio vascolare: stimolano l’attività della nitrossido sintasi endoteliale (eNOS), aumentando la produzione di ossido nitrico (NO). Il NO è un potente vasodilatatore che migliora il flusso sanguigno, abbassa la pressione arteriosa e favorisce l’ossigenazione cerebrale. Inoltre, i flavonoidi hanno un’azione antiossidante diretta (neutralizzazione dei radicali liberi) e indiretta (induzione di enzimi antiossidanti), proteggendo neuroni e cellule endoteliali dallo stress ossidativo. Alcuni studi clinici hanno dimostrato che il consumo regolare di cacao ricco in flavonoidi migliora la funzione endoteliale e le performance cognitive.
Ma non basta. Il piacere del cioccolato non è soltanto biochimico: è anche profondamente sensoriale. L’esperienza inizia già con l’udito, con quel caratteristico snap quando si spezza una tavoletta, un suono secco che ci anticipa la freschezza e la qualità del prodotto. Poi interviene il tatto: la superficie liscia sotto le dita e la resistenza al morso che cede gradualmente. In bocca il cioccolato si trasforma: il burro di cacao, unico tra i grassi per la sua particolare composizione, fonde a una temperatura vicinissima a quella corporea, regalando quella sensazione vellutata e avvolgente che sembra sciogliersi sulla lingua quasi senza sforzo.
A questo si aggiunge l’olfatto, forse il senso più importante: il calore della bocca libera lentamente centinaia di composti aromatici – dalle note tostate e leggermente amare delle pirazine, a quelle fruttate degli esteri, fino ai sentori di vaniglia o spezie che possono accompagnare certe miscele. Infine, il gusto completa l’esperienza con il suo equilibrio tra dolcezza, amaro e acidità, un gioco di contrasti che stimola le papille gustative e rende ogni morso appagante.
È proprio l’intreccio di queste percezioni – suono, tatto, vista, olfatto e gusto – che fa del cioccolato non solo un alimento, ma un piccolo rito multisensoriale, capace di trasformare un frammento di tavoletta in un momento di gratificazione e benessere.
Dalla percezione alla scienza
Negli ultimi decenni, il cioccolato è diventato anche un oggetto di ricerca scientifica. Non ci si limita a indagare perché ci fa sentire bene, ma si studiano le proprietà fisiche e chimiche che ne determinano qualità e stabilità: la cristallizzazione del burro di cacao, la viscosità del fuso, la texture al morso.
Tecniche avanzate come la calorimetria differenziale (DSC), la reologia e la risonanza magnetica a campo variabile (NMR relaxometria) permettono di esplorare come ingredienti diversi influenzino la struttura del cioccolato. Per esempio, come cambia quando si sostituisce lo zucchero con dolcificanti alternativi, o il latte con componenti vegetali per chi segue una dieta vegana o è intollerante al lattosio.
Una ricerca tutta italiana
Proprio sul tema con si è chiuso il paragrafo precedente, ho contribuito a uno studio pubblicato su European Food Research and Technology.
Con un gruppo di colleghi abbiamo confrontato cioccolati tradizionali con varianti vegane e a ridotto contenuto di zuccheri. I risultati hanno mostrato differenze misurabili:
- i cioccolati senza latte risultano meno duri e meno adesivi, con un comportamento reologico più fluido;
- quelli con zuccheri alternativi, invece, modificano la cristallizzazione del burro di cacao e aumentano la resistenza al flusso (yield stress);
- le analisi NMR hanno rivelato “impronte digitali” molecolari uniche, utili a distinguere le diverse formulazioni in modo rapido e non distruttivo.
Insomma, anche quando cambiano ingredienti e ricette, la scienza ci aiuta a garantire che il risultato finale sia comunque un cioccolato capace di dare piacere al palato.
Il futuro del cioccolato
Quello che emerge è un nuovo scenario: una generazione di cioccolati che non rinunciano al gusto, ma che cercano di conciliare benessere, salute e sostenibilità. Non si tratta più soltanto di un piacere edonistico, ma di un alimento che può dialogare con le esigenze nutrizionali moderne, con la ricerca di prodotti più etici e con una maggiore consapevolezza ambientale. La scienza, in questo percorso, ha un ruolo decisivo: dalle tecniche di fermentazione e tostatura che modulano aromi e consistenze, fino alle analisi sofisticate che permettono di comprendere e ottimizzare la struttura interna del cioccolato, rendendo possibile sperimentare nuove formulazioni senza sacrificare la qualità sensoriale.
Dal laboratorio al consumatore, la chimica diventa così uno strumento di innovazione culturale oltre che tecnologica, capace di custodire la tradizione e, allo stesso tempo, di aprire la strada a un futuro in cui il cioccolato possa essere non solo buono, ma anche sano e sostenibile.
E forse proprio qui sta il segreto della cioccolata: nel suo equilibrio perfetto tra storia e modernità, tra cultura e molecole, tra arte e scienza. Un equilibrio che continua a rinnovarsi e a sorprenderci, rendendo ogni morso non soltanto un piccolo piacere quotidiano, ma anche la testimonianza di un legame profondo fra uomo, natura e conoscenza.
Riferimenti & Approfondimenti
Barišić, V.; Kopjar, M.; Jozinović, A.; Flanjak, I.; Ačkar, Đ.; Miličević, B.; Šubarić, D.; Jokić, S.; Babić, J. (2019) The Chemistry behind Chocolate Production. Molecules 24: 3163. https://doi.org/10.3390/molecules24173163
BBC (2019) A brief history of chocolate
Encyclopedia Britannica Chocolate
Fredholm, B.B.; Bättig, K.; Holmén J.; Nehlig, A.; Zvartau, E.E. (1999) Actions of caffeine in the brain with special reference to factors that contribute to its widespread use. Pharmacol Rev. 51(1): 83-133. https://pubmed.ncbi.nlm.nih.gov/10049999/
Sabelli, H.; Fink, P.; Fawcett, J.; Tom, C. (1996) Sustained antidepressant effect of PEA replacement. J Neuropsychiatry Clin Neurosci 8: 168-71. https://doi.org/10.1176/jnp.8.2.168
Schroeter, H. ; Heiss, C.; Balzer, J.; Kleinbongard, P. ; Keen, C.L.; Hollenberg, N.K.; Sies, H.; Kwik-Uribe, C.; Schmitz, H.H.; Kelm, M. (2006) (–)-Epicatechin mediates beneficial effects of flavanol-rich cocoa on vascular function in humans, Proc. Natl. Acad. Sci. 103 (4) 1024-1029. https://doi.org/10.1073/pnas.0510168103
Torregrossa, F.; Cinquanta, L.; Albanese, D.; Cuomo, F.; Librici, C.; Lo Meo, P.; Conte, P. (2024) Vegan and sugar-substituted chocolates: assessing physicochemical characteristics by NMR relaxometry, rheology, and DSC. Eur Food Res Technol 250: 1219–1228. https://doi.org/10.1007/s00217-023-04457-w
Note
[1] Il termine “conching” deriva dall’inglese conch (conchiglia), per via della forma delle prime macchine impiegate. Si tratta di un processo introdotto nel 1879 da Rodolphe Lindt: la massa di cioccolato viene agitata e mescolata per ore a temperatura controllata, così da eliminare aromi indesiderati, affinare le particelle solide e rendere il cioccolato più vellutato e cremoso, con il tipico effetto “melt-in-the-mouth”.