Avete presente i gas nobili? Sono quelli dell’ultimo gruppo della tavola periodica (riquadro in rosso di Figura 1).
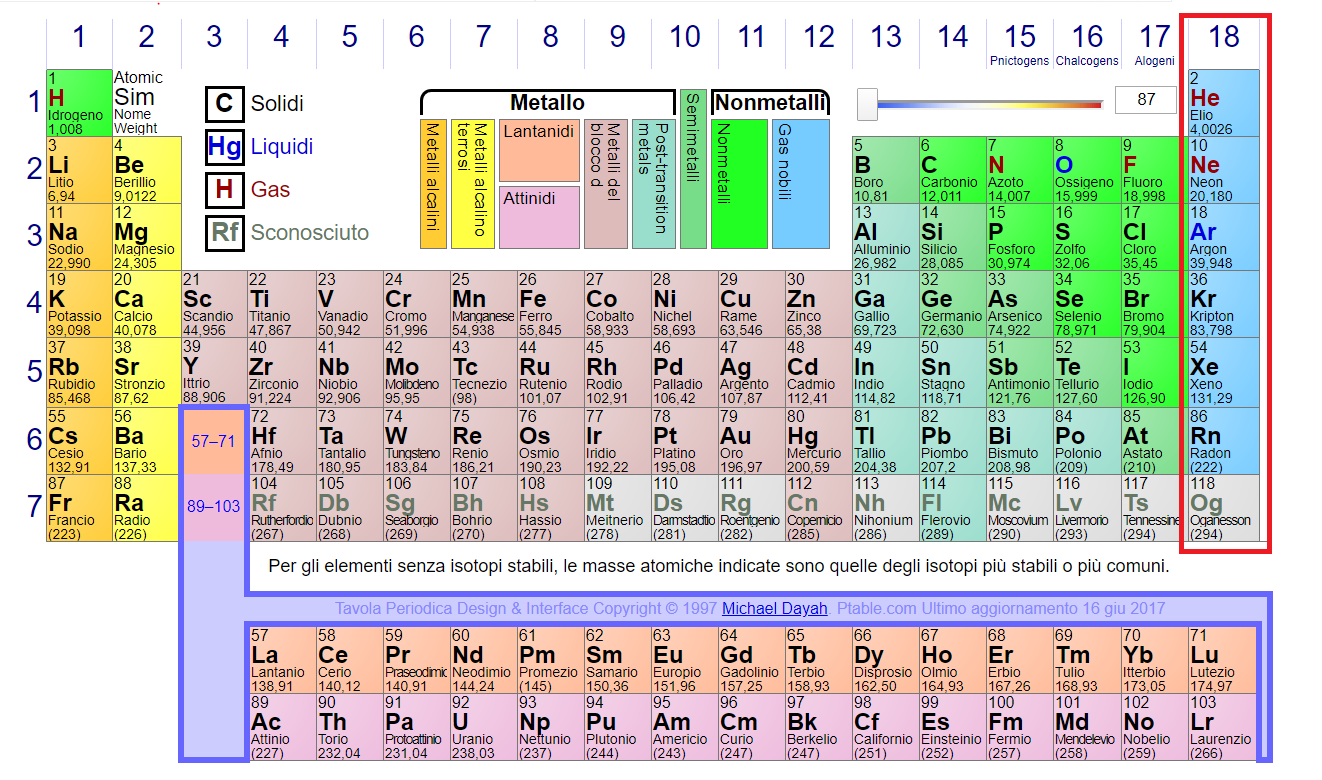
Fin da quando cominciamo a frequentare le scuole superiori (lo so…oggi non si chiamano più così…ma lasciatemi il vezzo di chiamarle ancora nel modo noto quando le frequentavo) ci viene insegnato che i gas nobili prendono questo nome perché sono altezzosi, hanno la puzza sotto al naso…ovvero incarnano lo stereotipo dei nobili dal punto di vista dei popolani: non frequentano nessuno. Chimicamente vuol dire semplicemente che sono non reattivi. A differenza di tutti gli altri elementi della tavola periodica, Elio, Neon, Argo, Cripto, Xeno e Radon non si combinano con nessun altro elemento.
Ma ne siamo veramente sicuri?
No. In effetti non è così. Diciamo pure che, quando ho cominciato i miei studi di Chimica (nell’ormai lontano 1986), un composto dello Xeno era già stato sintetizzato. Nel 1962, infatti, Neil Bartlett riuscì ad ottenere l’esafluoroplatinato di Xeno (XePtF6). La Figura 2 mostra il lavoro di Bartlett pubblicato sui Proceedings of the Chemical Society.

Quindi, possiamo dire che a partire dal 1962 non si può più dire che i gas nobili siano inerti. Ce ne è almeno uno, lo Xeno, che forma dei composti.
Ma è l’unico?
No, non è l’unico. Facciamo un salto temporale: 1962-2019. Sono passati 57 anni. Ci sono voluti tutti questi anni per ottenere un nuovo composto da un gas nobile. Stavolta si tratta dell’Argo. E’ stato utilizzato in condizioni molto diverse da quelle in cui siamo adatti a vivere per ottenere una lega col Nickel (ArNi). Non ci credete? Ebbene, cliccate sulla figura qui sotto.
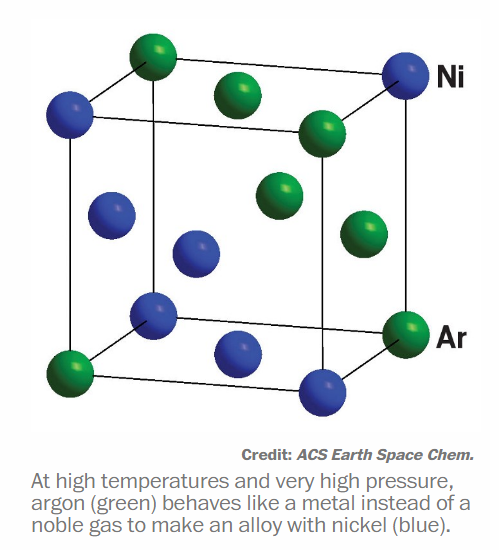
Alla fine i gas nobili sono come Superman. Hanno i superpoteri solo quando sono sulla Terra. Se si cambiano le condizioni (come per esempio Superman in presenza della kryptonite), perdono la loro nobiltà e si comportano come dei “volgari” metalli.
Fonte dell’immagine di copertina